猪德尔塔冠状病毒(porcine deltacoronavirus, PDCoV)是一种致病性猪肠道冠状病毒,能够感染包括人类在内的多种动物。研究发现,PDCoV可利用多物种来源的APN同源物作为受体入侵宿主细胞,包括人源APN(hAPN)和猪源APN(pAPN)。2021年,《Nature》杂志报道在海地三名儿童血浆样本中分离出PDCoV毒株,引发了人们对其潜在人畜共患风险的高度关注。结构生物学研究表明,PDCoV的受体结合域(receptor-binding domain, RBD)在结合hAPN和pAPN时具有高度保守性,并且对hAPN的结合亲和力高于pAPN。然而,PDCoV尚未在人群中造成大规模传播,这提示其通过hAPN与pAPN介导的感染效率仍存在差异,但其分子机制尚不明确。
近日,兽医所动物腹泻病防控创新团队与南京农业大学刘斐教授团队,在中国科学院亚热带农业生态研究所印遇龙院士指导下,在 Science China Life Sciences (IF=9.5,一区TOP期刊)发表题为“Receptor affinity-selective differential dynamics of membrane fusion initiation govern deltacoronavirus cross-species transmission”的研究论文。该研究系统解析了PDCoV利用人源与猪源受体介导入侵不同宿主细胞时的动态机制,揭示了受体亲和力调节的膜融合启动动力学差异对于德尔塔冠状病毒感染及跨种传播具有决定性作用。

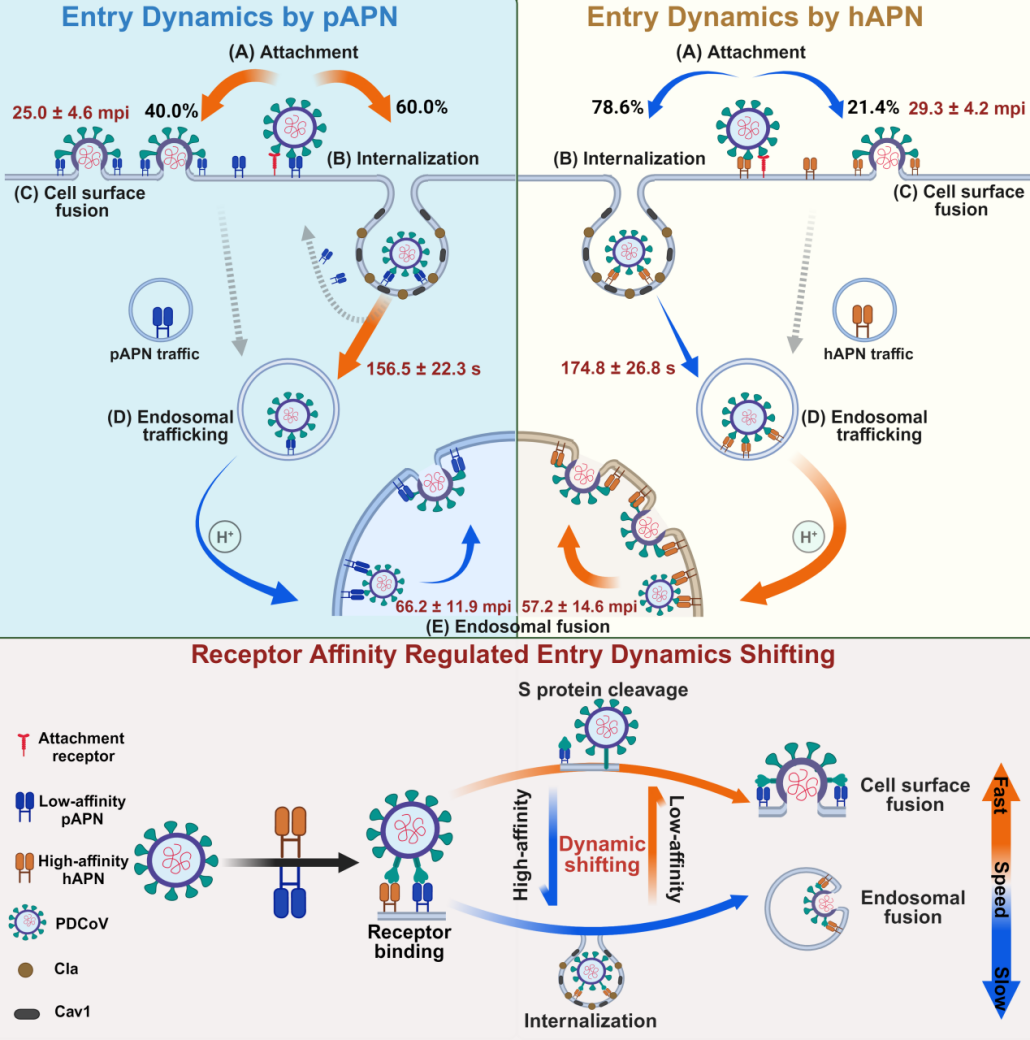
研究团队利用单病毒示踪技术,首次可视化了PDCoV通过hAPN和pAPN介导的内化过程。结果发现,虽然hAPN和pAPN几乎同时结合PDCoV,但pAPN介导的内化速度显著快于hAPN,提示PDCoV经由pAPN入侵时能更高效地进入细胞。进一步分析显示,两种受体启动的膜融合动力学也存在明显差异:pAPN触发的细胞表面融合速度更快、频率更高,有助于PDCoV迅速建立感染;而hAPN则更易诱导快速且高频率的内体融合,有利于病毒逃避免疫识别。此外,研究还表明,两种受体均可通过网格蛋白介导及小窝介导的内吞作用完成PDCoV内化,其中小窝介导的内吞更为高效。通过引入多种降低APN-RBD亲和力的hAPN突变体,研究最终证实PDCoV RBD与APN同源物之间的结合亲和力是调节上述差异性动力学的关键因素,从而驱动PDCoV在两种融合路径之间灵活切换。
综上,该研究阐明了PDCoV利用APN同源物跨种传播的动态差异机制,强调受体亲和力对入侵动力学的调节作用对于病毒在快速感染与免疫逃逸之间实现平衡至关重要,并为德尔塔冠状病毒种间传播的进化策略提供了新的分子见解。
本研究的第一作者为南京农业大学动物医学院博士研究生安达,兽医所李彬研究员、南京农业大学刘斐教授、单衍可博士和中科院亚热带农业生态研究所印遇龙院士为论文的共同通讯作者。该项目得到国家自然科学基金、江苏省农业科技自主创新资金等项目资助。